В уроке 13 «» из курса «Химия для чайников » рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
В результате реакции горения метана CH 4 в кислороде O 2 образуются диоксид углерода CO 2 и вода H 2 O. Эта реакция может быть описана химическим уравнением :
- CH 4 + O 2 → CO 2 + H 2 O (1)
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O 2 расходуется в расчете на 1 молекулу CH 4 и сколько молекул CO 2 и H2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
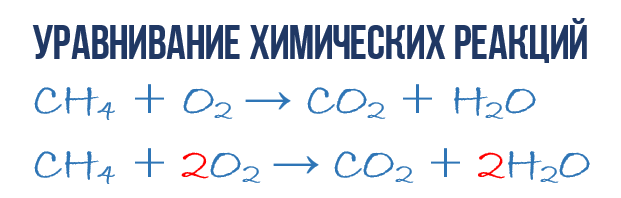
Начнем с углерода. В левой части один атом С входит в состав молекулы CH 4 , а в правой части один атом С входит в состав CO 2 . Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
- 1CH 4 + O 2 → 1CO 2 + H 2 O (2)
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H 4 = 4H) в составе молекулы CH 4 , а в правой – всего 2 атома H в составе молекулы H 2 O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H 2 O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
- 1CH 4 + O 2 → 1CO 2 + 2H 2 O (3)
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H 2 O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H 2 O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
- 1CH 4 + 2O 2 → 1CO 2 + 2H 2 O или СH 4 + 2O 2 → CO 2 + 2H 2 O (4)
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C 7 H 5 N 3 O 6 энергично соединяется с кислородом, образуя H 2 O, CO 2 и N 2 . Запишем уравнение реакции, которое будем уравнивать:
- C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (5)
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
- 2C 7 H 5 N 3 O 6 + O 2 → 14CO 2 + 5H 2 O + 3N 2 (7)
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O 2 . Таким образом полное химическое уравнение будет иметь вид:
- 2C 7 H 5 N 3 O 6 + 10,5O 2 → 14CO 2 + 5H 2 O + 3N 2 (8)
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
- 4C 7 H 5 N 3 O 6 + 21O 2 → 28CO 2 + 10H 2 O + 6N 2 (9)
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
- C 7 H 5 N 3 O 6 + 5,25O 2 → 7CO 2 + 2,5H 2 O + 1,5N 2 (10)
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты , а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро N A =6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O 2 с образованием 28 молей CO 2 , 10 молей H 2 O и 6 молей N 2 .
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O2 = 31,999 г/моль
- CO2 = 44,010 г/моль
- H2 O = 18,015 г/моль
- N2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO 2 , 10·18,015 г = 180,15 г H 2 O и 6·28,013 г = 168,08 г N 2 . Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO2 | |
| 671,98 г CO2 | 180,15 г H2 O | |
| 168,08 г N2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2 :
- CaCO 3 + 2HCl → CaCl 2 + CO 2 + H 2 O (11)
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO 3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 . Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO 3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl 2 (110,99 г/моль), CO 2 (44,01 г/моль) и H 2 O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO 3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
- CaCO 3 (тв.) + 2H + (водн.) → Ca 2+ (водн.) + CO 2 (г.) + H 2 O(ж.) (12)
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO 3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO 2 и H 2 O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений » вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.
Составление химических формул для соединений двух химических элементов в тех случаях, когда для каждого элемента существует только одна стехиометрическая валентность.
|
Алгоритм действия |
Составление химической формулы оксида алюминия |
|
|
Установление (по названию соединения) химических символов элементов | ||
|
Определение валентности атомов элементов | ||
|
Указание числового отношения атомов в соединении | ||
|
Составление формулы |
Аl 2 О 3 |
|
Составление химических формул для соединений, которые существуют в водном растворе в виде ионов.
|
Алгоритм действия |
Составление химической формулы сульфата алюминия |
|
|
Установление (по названию соединения) химических формул ионов | ||
|
Определение числа зарядов ионов | ||
|
Вычисление наименьшего общего кратного | ||
|
Определение дополнительных множителей | ||
|
Указание числового отношения ионов | ||
|
Указание стехиометрических индексов | ||
|
Составление формулы |
Аl 2 (SО 4 ) 3 |
|
Написание химических формул
Для указания в химических формулах стехиометрических индексов и зарядов ионов существуют следующие правила.
1. Если стехиометрический индекс относится к группе атомов, обозначающие эту группу химические символы ставятся в скобки:
С 3 Н 5 (ОН) 3 – в молекуле глицерина содержатся 3 гидроксигруппы;
Ca(NО 3) 2 – в формульной единице нитрата кальция содержатся ионы кальция и нитрат-ионы в соотношении 1: 2.
2. Данные о заряде сложного многоатомного иона в химической формуле относятся ко всему иону:
SО 4 2– – сульфат-ион – имеет двухкратный отрицательный заряд;
NН 4 + – ион аммония – имеет одинарный положительный заряд.
3. Химическая формула комплексного иона ставится в квадратные скобки, за которыми указывается его заряд; она состоит из:
– химического символа центрального атома;
– химической формулы лиганда в круглых скобках;
– нижнего индекса, указывающего число лигандов.
4– – гексацианоферрат(II)-ион; в имеющем четыре отрицательных заряда ионе шесть лигандов СN – (цианид-ион) связаны с центральным атомом Fе II (катион железа Fe 2+).
2+ – ион тетраамминмеди (II); в имеющем два положи-тельных заряда ионе четыре лиганда NH 3 (молекула аммиака) связаны с центральным атомом меди (ион Сu 2+).
4. Химическая формула воды в гидратах и кристаллогидратах отделяется точкой от химической формулы основного вещества.
CuSO 4 · 5H 2 O – пентагидрат сульфата меди (II) (медный купорос).
Классификация неорганических веществ и их свойства
Все неорганические вещества делятся на простые и сложные.
Простые вещества подразделяются на металлы, неметаллы и инертные газы.
Важнейшими классами сложных неорганических веществ являются: оксиды, основания, кислоты, амфотерные гидрооксиды, соли.
Оксиды - это соединения двух элементов, один из которых кислород. Общая формула оксидов:
Э m O n
где m – число атомов элемента Э;
n – число атомов кислорода.
Примеры оксидов: К 2 О, CaO, SO 2 , P 2 O 5
Основания – это сложные вещества, молекулы которых состоят из атома металла и одной или нескольких гидроксидных групп – ОН. Общая формула оснований:
Me (ОН) y
где у – число гидроксидных групп, равное валентности металла (Me).
Примеры оснований: NaOH, Ca(OH) 2 , Со(ОН) 3
Кислоты - это сложные вещества, содержащие атомы водорода, которые могут замещаться атомами металла.
Общая формула кислот
Н х Ас у
где Ас – кислотный остаток (от англ., acid – кислота);
х – число атомов водорода, равное валентности кислотного остатка.
Примеры кислот: НС1, HNO 3 , H 2 SO 4 , H 3 PO 4
Амфотерные гидроксиды – это сложные вещества, которые имеют свойства кислот и свойства оснований. Поэтому формулы амфотерных гидроксидов можно записывать в форме оснований и в форме кислот. Примеры амфотерных гидроксидов:
Zn(OH) 2 = H 2 ZnO 2
Al(OH) 3 = H 3 AlO 3
форма форма
оснований кислот
Соли – это сложные вещества, которые являются продуктами замещения атомов водорода в молекулах кислот атомами металла или продуктами замещения гидроксидных групп в молекулах оснований кислотными остатками. Например:
Состав нормальных солей выражается общей формулой:
Ме х (Ас) у
где х - число атомов металла; у - число кислотных остатков.
Примеры солей: K 3 PO 4 ; Mg SO 4 ; Al 2 (SO) 3 ; FeCl 3.
Оксиды
Например: СО – оксид углерода (II) – (читается: "оксид углерода два"); СО 2 – оксид углерода (IV); Fe 2 O 3 – оксид железа (III).
Если элемент имеет постоянную валентность, ее в названии оксида не указывают. Например: Nа 2 О – оксид натрия; Аl 2 О 3 – оксид алюминия.
Классификация
Все оксиды делятся на солеобразующие и несолеобразующие (или индифферентные).
Несолеобразующие (индифферентные) оксиды - это оксиды, которые не образуют солей при взаимодействии с кислотами и основаниями. Их немного. Запомните четыре несолеобразующих оксида: СО, SiO, N 2 O, NO.
Солеобразующие оксиды - это оксиды, которые образуют соли при взаимодействии с кислотами или основаниями. Например:
Na 2 O + 2НС1 = 2NaCl + Н 2 О
оксид кислота соль
Некоторые оксиды с водой не взаимодействуют, но им соответствуют гидроксиды, которые можно получить косвенным (непрямым) путем. В зависимости от характера соответствующих гидроксидов все солеобразующие оксиды делятся на три типа: основные, кислотные, амфотерные.
Основные оксиды - это оксиды, гидраты которых являются основаниями. Например:
В уроке рассматривается алгоритм составления химических формул веществ по известным валентностям химических элементов. Учитель объяснит два разных способа вывода химической формулы вещества.
2. определим число общих единиц валентности, оно равно наименьшему общему кратному валентностей элементов: НОК (2,4)= 4;
3. определим число атомов каждого химического элемента в молекуле, разделив число общих единиц валентности на валентность элемента;
4. запишем формулу вещества: SO 2 .
Пример 2 . Составим формулу вещества, образованного атомами фосфора (с валентностью V) и атомами кислорода.
1. Запишем знаки элементов и над ними укажем их валентности: .
2. Найдем число общих единиц валентности: НОК(2,5)=10
3. Найдем число атомов фосфора в молекуле: 10:5=2.
4. Найдем число атомов кислорода в молекуле: 10:2=5.
5. Запишем формулу вещества: .

Рис. 2. Составление химической формулы оксида фосфора
1. Емельянова Е.О., Иодко А.Г. Организация познавательной деятельности учащихся на уроках химии в 8-9 классах. Опорные конспекты с практическими заданиями, тестами: Часть I. - М.: Школьная Пресса, 2002. (с.33)
2. Ушакова О.В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006. (с. 36-38)
3. Химия: 8-й класс: учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005.(§16)
4. Химия: неорг. химия: учеб. для 8 кл. общеобразоват. учреждений / Г.Е. Рудзитис, Ф.Г. Фельдман. - М.: Просвещение, ОАО «Московские учебники», 2009. (§§11,12)
5. Энциклопедия для детей. Том 17. Химия / Глав. ред.В.А. Володин, вед. науч. ред. И. Леенсон. - М.: Аванта+, 2003.
Дополнительные веб-ресурсы
1. Единая коллекция цифровых образовательных ресурсов ().
2. Электронная версия журнала «Химия и жизнь» ().
Домашнее задание
1. с.84 №№ 3,4 из учебника «Химия: 8-й класс» (П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005).
2. с. 38 № 9 из Рабочей тетради по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006.
Тип урока. Комбинированный.
Методы обучения. Частично поисковый.
Цели. Дидактическая: закрепить понятие “валентность”, навыки определения валентности по формуле и Периодической таблице.
Психологическая: вызвать интерес к предмету, выработать умение логически рассуждать, грамотно выражать свои мысли.
Воспитательная: развивать умение работать коллективно, оценивать ответы своих товарищей.
Оборудование. Наборы для построения моделей молекул различных веществ, таблички-анаграммы для химической разминки, мишень эффективности
ХОД УРОКА
1. Ориентировочно-мотивационный этап
Химическая разминка
Анаграммы – это слова, в которых изменен порядок букв. Попробуйте разгадать некоторые из химических анаграмм. Переставьте буквы в каждом слове и получите название химического элемента. Обратите внимание на подсказку.
“Одоврод” – у этого элемента самая маленькая относительная атомная масса.
“Маилинюй” – этот элемент называют “крылатым” металлом.
“Дикосолр” – входит в состав воздуха.
“Цалький” – без него наши кости были бы непрочными и хрупкими.
“Озежел” – этот элемент входит в состав крови и участвует в переносе кислорода.
Учитель. Если вы легко разгадали слова-анаграммы, скажите себе: “Я – молодец!”
2. Актуализация знаний
Лови ошибку (Ребята ищут ошибку, работают парами, спорят, совещаются. Придя к какому-то мнению, предлагают свой аргументированный вариант ответа)
Слово “валентность”(от лат. “valentia”) возникло в середине XIX в., в период завершения химико-аналитического этапа развития химии. “Валентность – способность атомов одного элемента присоединять определенное количество атомов другого элемента”. С одним атомом одновалентного элемента соединяется один атом другого одновалентного элемента (HF, NaCl). С атомом двухвалентного элемента соединяются один атом одновалентного (H 2 O) или один атом двухвалентного (CaO). Значит, валентность элемента можно представить как число, которое показывает, со сколькими атомами одновалентного элемента может соединяться атом данного элемента.
Есть элементы, которые имеют постоянную
валентность:
одновалентны (I) - H, Li, Na, Rb, Cs, F, I
двухвалентны (II) - Be, Mg, Ca, Sr, Ba, Zn, Cd K
трехвалентны (III) - B, Al, O
Крестики нолики: (Соедините элементы прямой, критерий правильного ответа – постоянная валентность выбранных элементов)
1 вариант
2 вариант
3. Изучение новых знаний
Задание 1: дана общая формула соединения водорода с каким-либо элементом
Зная, что валентность водорода равна I, определите валентность элемента.
Ребята работают парами, при необходимости объединяются в четвёрки, спорят, совещаются. Придя к какому-то мнению, предлагают свой аргументированный вариант ответа. В результате получаем схему №1
схема 1
Задание для закрепления:
- определите валентности элементов в соединениях с водородом: PH 3 , HF, H 2 S, CaH 2 ,
- назовите соединения.
Задание 2: таким же способом можно определить валентности элементов в соединениях с кислородом зная, что кислород двухвалентен. Например:
Ребята работают парами, при необходимости объединяются в четвёрки, спорят, совещаются. Придя к какому-то мнению, предлагают свой аргументированный вариант ответа. В результате получаем схему №2
 схема
2
схема
2
Задание для закрепления:
- определите валентности элементов в соединениях с кислородом:
- Как называются бинарные соединения, содержащие кислород?
NO 2 , N 2 O 5 , SO 2 , SO 3 , Cl 2 O 7 .
Задание 3: что же нужно обязательно знать, чтобы определить валентность элементов в бинарном соединении? (валентность одного из элементов)
Определите валентность атомов в соединении
Ребята работают парами, при необходимости объединяются в четвёрки, спорят, совещаются. Придя к какому-то мнению, предлагают свой аргументированный вариант ответа. В результате получаем схему №3

Учитель: какая из приведённых схем
 схема
2
схема
2

наиболее полно отражает правило определения валентности по формуле? (схема 3, т.к.она отражает общий случай, а схемы 1 и 2 лишь частные)
4. Закрепление изученного материала.
Самостоятельная работа
Текст работы заранее написан на доске. Двое учащихся решают задание на обратной стороне доски, остальные в тетрадях.
Задание 4. Проверьте, правильно ли написаны формулы следующих соединений: Na 2 S, KBr, Al 2 O 3 , Mg 3 N 2 , MgO.
5. Обобщение и систематизация знаний.
Творческая работа в группах
Задание 5. Используя наборы для составления моделей молекул различных веществ, составьте формулы и модели молекул для следующих соединений:
1-я группа – меди и кислорода,
2-я группа – цинка и хлора,
3-я группа – калия и йода,
4-я группа – магния и серы.
После окончания работы один учащийся из группы отчитывается о выполненном задании и вместе с классом проводит анализ ошибок.
Задание 6. Напишите формулы соединений металлов с неметаллами: кальция с кислородом, алюминия с хлором, натрия с фосфором. Назовите эти соединения.
После выполнения работы ученики обмениваются тетрадями, происходит взаимопроверка.
Задание 7. Запишите порядок действия при составлении формул веществ, анализируя предложенный пример
Порядок действия |
|
6. Рефлексия
У Вас есть возможность сделать самооценку своей деятельности на уроке. Вам предлагается “Мишень эффективности”.
Отметьте свои знания по новой теме, отметив на рисунке соответствующий им сектор штриховкой. Сдайте свои записи.

7. Домашнее задание. По учебнику “Химия-8” (УМК Кузнецова Н.Е. и др.) § 14, упражнение1-71 обязательное (дополнительные с 1-72 по 1-74).
Сообщения о французском ученом Ж.Л.Прусте и английском ученом Дж.Дальтоне.
Литература
- Кузнецова Н.Е. и др. Химия: Учебник для учащихся 8 класса общеобразовательных учреждений.- М.: Вентана-Граф, 2010. – 320с.: ил.
- Кузнецова Н.Е., Шаталов М.А. Обучение химии на основе межпредметной интеграции: 8-9 классы: Учебно-методическое пособие.- М.: Вентана-Граф, 2004. – 352с.
- Емельянова Е.О., Иодко А.Г. Организация познавательной деятельности учащихся на уроках химии в 8-9 классах. Опорные конспекты с практическими заданиями, тестами: В 2-х частях. Часть I.– М.: Школьная пресса, 2002.- 144с.
- Кузнецова Л.М. Новая технология обучения химии в 8 классе.- Обнинск: Титул,1999.- 208с.:ил
Одной из самых главных задач в химии является правильное составление химических формул. Химическая формула — это письменное представление состава химического вещества с помощью латинского обозначения элемента и индексов. Для правильного составления формулы нам обязательно понадобится таблица Менделеева и знание простых правил. Они достаточно простые и запомнить их смогут даже дети.
Как составлять химические формулы
Основным понятием при составлении химических формул является «валентность «. Валентность — это свойство одного элемента удерживать определенное число атомов в соединении. Валентность химического элемента можно посмотреть в таблице Менделеева, а также нужно помнить и уметь применять простые общие правила.
- Валентность металла всегда равна номеру группы, при условии, что он находится в главной подгруппе. Например, калий имеет валентность 1, а кальций — 2.
- С неметаллами немного сложнее. Неметалл может иметь высшую и низшую валентности. Высшая валентность равна номеру группы. Низшую валентность можно определить вычтя номер группы элемента из восьми. При соединении с металлами неметаллы всегда имеют низшую валентность. Кислород всегда имеет валентность 2.
- В соединении двух неметаллов низшую валентность имеет тот химический элемент, который находится в таблице Менделеева правее и выше. Однако, фтор всегда имеет валентность 1.
- И еще одно важное правило при расстановке коэффициентов! Общее число валентностей одного элемента всегда должно быть равно общему количеству валентностей другого элемента!
Закрепим полученные знания на примере соединения лития и азота. Металл литий имеет валентность, равную 1. Неметалл азот располагается в 5 группе и имеет высшую валентность 5 и низшую — 3. Как мы уже знаем, в соединениях с металлами неметаллы всегда имеют низшую валентность, поэтому азот в данном случае будет иметь валентность равную трем. Расставляем коэффициенты и получаем искомую формулу: Li 3 N.
Вот так, достаточно просто, мы научились составлять химические формулы! А для лучшего запоминания алгоритма составления формул мы подготовили его графическое представление.









